美國成熟卵母細胞紡錘體兼容大部分顯微鏡
在核移植過程中,紡錘體的穩定性是首要考慮的問題。冷凍和解凍過程中的溫度變化和冷凍保護劑的毒性都可能對紡錘體造成損傷,導致染色體分離異常,進而影響胚胎發育。因此,如何在冷凍過程中保持紡錘體的穩定性,是核移植紡錘體卵冷凍研究面臨的重要挑戰。體細胞核在移入去核卵母細胞后,需要經歷復雜的重新編程過程,以獲得全能性。然而,這一過程受到多種因素的調控,包括表觀遺傳修飾、轉錄因子表達等。在冷凍過程中,這些調控機制可能受到干擾,導致重新編程失敗或異常,從而影響胚胎發育。紡錘體的微管在細胞分裂過程中具有自我修復和再生的能力。美國成熟卵母細胞紡錘體兼容大部分顯微鏡
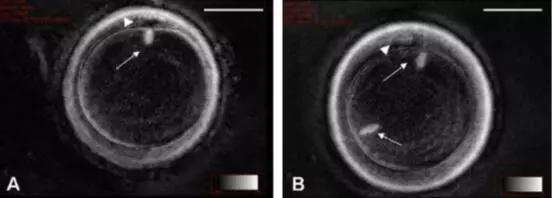
帕金森病是一種以多巴胺能神經元丟失為主要特征的神經退行性疾病,其主要病理特征是α-突觸蛋白的異常聚集。研究表明,紡錘體功能障礙在帕金森病的發生和發展中也起著重要作用。帕金森病患者中,微管蛋白的突變和異常磷酸化會影響微管的穩定性和紡錘體的組裝,導致染色體分離異常和細胞周期紊亂。紡錘體功能障礙會影響線粒體的正常運輸和分布,導致線粒體功能障礙,進一步加劇神經元的損傷和死亡。紡錘體功能障礙會導致細胞周期紊亂,增加細胞凋亡的風險,加速神經元的丟失。ICSI紡錘體卵冷凍研究紡錘體微管的動態不穩定性是其功能的基礎。
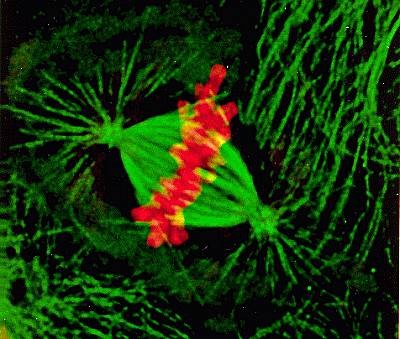
微管重組技術是體外構建紡錘體模型的基礎。通過在體外重組微管蛋白,可以形成類似于細胞內紡錘體的微管結構。常見的方法包括:從牛腦或其他來源中純化微管蛋白,確保其純度和活性。在體外條件下,通過控制溫度、離子濃度等參數,誘導微管蛋白組裝成微管。使用微管穩定劑(如紫杉醇)或調節蛋白(如MAPs)穩定微管結構,模擬細胞內的微管動態變化。動力蛋白和調節蛋白是紡錘體功能的重要組成部分。通過在體外模型中添加這些蛋白,可以模擬紡錘體的動力學行為。常見的方法包括:添加動力蛋白(如dynein、kinesin)以模擬微管的運動和動力學行為。添加調節蛋白(如AuroraB、Mad2)以模擬紡錘體檢查點的功能。
紡錘體的異常與多種疾病的發生和發展密切相關。例如,紡錘體形成或功能缺陷可能導致染色體分離錯誤,進而引發遺傳性疾病的發生。此外,紡錘體異常還可能影響細胞的增殖和分化能力,導致細胞增殖失控的發生。因此,深入研究紡錘體的形成機制和功能,對于揭示細胞分裂的調控機制、預防相關疾病具有重要意義。紡錘體作為有絲分裂過程中的精密“導航儀”,在細胞分裂中發揮著至關重要的作用。其結構、形成機制、功能以及精密導航作用的研究,不僅有助于揭示細胞分裂的復雜過程,還為預防相關疾病提供了新的思路和方法。未來,隨著細胞生物學和分子生物學技術的不斷發展,相信我們將對紡錘體的工作機制有更深入的認識和理解,為細胞分裂調控機制的研究和疾病提供更多的理論依據和實踐指導。紡錘體的研究對于開發新的抗病毒藥物具有重要意義。
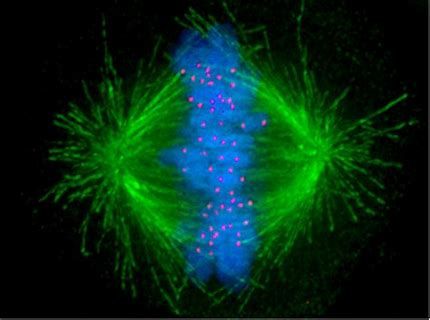
隨著科技的進步,冷凍與解凍技術也在不斷創新。例如,玻璃化冷凍技術因其快速冷凍和解凍的特點,能夠有效減少冷凍過程中的冰晶形成和滲透壓變化對紡錘體的損傷。此外,一些研究者還嘗試將微流控技術應用于卵母細胞的冷凍保存中,以實現更精確的溫度控制和更均勻的冷凍保護劑分布。無損觀察技術如偏光顯微鏡(Polscope)和冷凍電鏡(Cryo-EM)等的應用為MI期紡錘體卵冷凍研究提供了新的視角。這些技術能夠在不破壞卵母細胞活性的情況下實時觀察紡錘體的形態和變化,從而更準確地評估冷凍保存的效果。紡錘體微管的排列方向決定了染色體分離的方向。美國Hamilton Thorne紡錘體卵質量評估
紡錘體的結構和功能在不同類型的細胞中可能存在差異。美國成熟卵母細胞紡錘體兼容大部分顯微鏡
在有絲分裂中,紡錘體的形成與功能至關重要。首先,在有絲分裂前期,中心體復制并分離至細胞兩極,形成紡錘體的兩極。隨后,微管從兩極向中心區域延伸,形成紡錘體的主干。在中期,染色體在紡錘絲的牽引下,自動在赤道板排列整齊。當細胞進入分裂后期,紡錘體微管收縮,將染色體牽引至兩極,形成兩組數目相等的姐妹染色單體。這一過程確保了遺傳信息的準確傳遞,避免了染色體分離錯誤導致的遺傳異常。此外,紡錘體還決定了胞質分裂的分裂面。在染色體分裂的同時,紡錘體中的一部分微管不隨染色體分裂到兩極,而是停弛在紡錘體中心,形成紡錘中心體。紡錘中心體的中心區域為兩組極性相反的微管交疊區,稱為紡錘中心區,它決定了接下來的胞質分裂面。胞質分裂開始于分裂后期的較晚期,一般結束于分裂末期后1-2小時,此期間兩個子細胞由中心顆粒體連接。紡錘體通過精確控制胞質分裂面的位置,確保了細胞分裂的對稱性和穩定性。美國成熟卵母細胞紡錘體兼容大部分顯微鏡
- 上海哺乳動物紡錘體透明帶 2025-05-17
- 上海MII期紡錘體胚胎植入 2025-05-17
- 昆明Hamilton Thorne紡錘體揭示卵母細胞關鍵結構 2025-05-17
- 香港MII期紡錘體廠家 2025-05-17
- 香港成熟卵母細胞紡錘體改善分級 2025-05-17
- 上海MII期紡錘體價格 2025-05-17
- 武漢輔助生殖紡錘體加熱臺 2025-05-17
- 上海克隆紡錘體揭示卵母細胞關鍵結構 2025-05-17
- 武漢無需染色紡錘體價格 2025-05-16
- 昆明紡錘體提高冷凍保存效率 2025-05-16
- 浙江BIM-7402U 積分球型光電管功率計探測器銷售 2025-05-17
- 奧林巴斯便攜式XRF礦物探勘成分光譜分析儀 2025-05-17
- 云浮鏡片批發 2025-05-17
- 四川臭氧色牢度測試儀性價比高 2025-05-17
- 上海實驗室搬遷物流如何協調 2025-05-17
- 山東導波雷達液位計特點 2025-05-17
- 山西可靠性滴水試驗裝置供應商 2025-05-17
- 通用數顯儀HZS-81-02-03-00生產 2025-05-17
- 江蘇雷達物液位計價格 2025-05-17
- 浙江手持式多通道紫外成像儀商家 2025-05-17